①按照物质类别对上述反应中的各物质进行分类,未涉及的物质类别是(填序号)。
A.金属氧化物 B.非金属氧化物 C.酸 D.盐
②发生还原反应的产物是(写化学式);该反应(填“能”或“不能”)用稀硫酸代替盐酸。
|
|
| a |
| b | c |
d |
| e |
|
|
| f |

操作 | 现象 | 结论或离子方程式 |
步骤1:取少量滤液a进行①(填实验名称)。 | 火焰呈②。 | 滤液a中含有 |
步骤2:另取少量滤液a于试管中,依次滴入③(填化学式)溶液和氯水。 | 溶液先无红色,后变红色。 | 滤液a中含有 |
查阅资料,计算氧化
脱氢反应的反应热
i.查阅的燃烧热数据(填化学式)
ii.查阅水的汽化热:
利用上述数据,得如下热化学方程式:
反应Ⅰ
反应Ⅱ
反应Ⅲ
①反应Ⅱ自发进行的条件是(填“高温”“低温”或“任意温度”)。
②反应Ⅲ在热力学上趋势大于反应Ⅰ,其原因是。

①图中代表的物质是。
②曲线在250℃之后随温度升高而增大的原因是。
③250℃时,反应Ⅰ的平衡常数=。
①
②
过程①的平衡常数 , 其中
表示溶液中的
浓度,
表示大气中
的分压(单位:kPa)。其他条件不变时,温度升高,
(填“增大”或“减小”);当大气压强为
, 溶液中的
时(忽略
和水的电离),大气中
的体积分数为%(用含
,
、
、
的字母表示)。

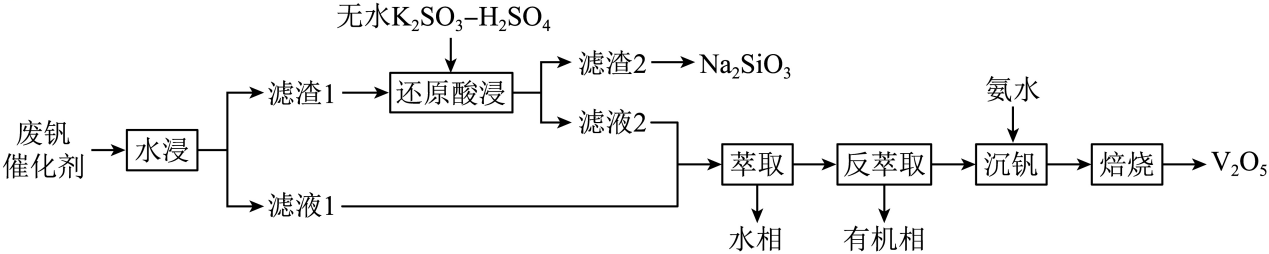
已知:钒的氧化物在酸性条件下以、
存在,
增大时
可转化为
沉淀。
①硫酸的用量会影响钒的浸出率,需保持在1.2以下的原因是。
②过程中除了有被还原成
, 还涉及的反应离子方程式为。
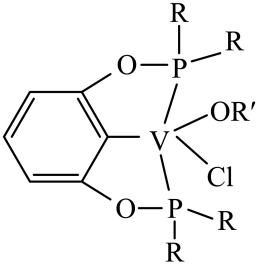
③若以磷酸为介质处理废催化剂,可以提高钒的浸出率。一种钒磷配合物的结构如图所示,形成配位键时V提供(选填“孤对电子”或“空轨道”)。